
ก่อนหน้านี้พี่กริฟฟินได้พาน้อง ๆ ไปทำความรู้จักกับหัวข้อการสอบของรายวิชา GED Science ในส่วนหัวข้อของ “โครงสร้างเซลล์” ที่เป็นหนึ่งในโจทย์สำคัญของข้อสอบ Biology (ชีววิทยา) และเนื้อหาเรื่อง “วิทยาศาสตร์โลกและอวกาศ” (Earth & Space Science) กันไปเป็นที่เรียบร้อย วันนี้ก็มาถึงคิวของหัวข้อ “ฟิสิกส์” (Physical Science) ซึ่งหัวข้อที่จะมาเจาะลึกในวันนี้ก็ได้แก่เรื่องของ “โมเลกุล” และ “อะตอม” นั่นเอง ถ้าใครอยากทราบว่าโมเลกุลคืออะไร ต่างจากอะตอมอย่างไร และจำเป็นยังไงกับการสอบ GED Science ก็ไปอ่านกันต่อได้เลย
ข้อสอบ GED Science หัวข้อ Physical Science ออกสอบอะไรบ้าง
สำหรับข้อสอบ GED Science ในหัวข้อ Physical Science ก็ถือว่าเป็นหนึ่งในหัวข้อใหญ่ของการสอบ GED Science เลย เพราะมีจำนวนข้อสอบถึง 40% ของตัวข้อสอบทั้งหมด ซึ่งเมื่อคิดจากสัดส่วนของข้อสอบทั้งหมดที่มีจำนวน 38 ข้อ ก็จะมีข้อสอบ Physical Science อยู่ที่ 13 – 16 ข้อเลยทีเดียว โดยข้อสอบในหัวข้อฟิสิกส์ก็จะประกอบไปด้วยคำถามเกี่ยวกับอะตอม โมเลกุล กระบวนการทางเคมี พลังงาน มวล การเคลื่อนที่และแรง คลื่น ไฟฟ้า สนามแม่เหล็ก ตลอดจนสสารและสถานภาพของสสารต่าง ๆ
มาถึงตรงนี้ น้องบางคนอาจจะสงสัยว่าทำไมในหัวข้อ “ฟิสิกส์” (Physics) ของข้อสอบ GED Science ถึงมีเนื้อหาที่เกี่ยวข้องกับเคมี (Chemistry) อยู่หลายส่วน นั่นก็เป็นเพราะการแบ่งหัวข้อการสอบใน GED Science ได้รวมเอาเนื้อหาด้านเคมีและฟิสิกส์เข้าด้วยกัน เนื่องจากสูตรทางเคมีหลายอย่างก็ต้องอาศัยการคิดคำนวณมารวมอยู่ด้วยนั่นเอง และในวันนี้พี่กริฟฟินก็จะพาน้อง ๆ มาเจาะลึกในหัวข้อ “อะตอมและโมเลกุล” กัน
อะตอมคืออะไร ?
Atom หรือ อะตอม คือ อนุภาคที่เล็กที่สุดของธาตุที่ยังแสดงลักษณะของธาตุนั้น ๆ ออกมาได้อย่างครบถ้วน โดยคำว่า atom มาจากภาษากรีกว่า “atomos” ซึ่งคำว่า “a” แปลว่า “ไม่” ส่วน “tomos” แปลว่า “แบ่งได้” นั่นเอง รวมกันจึงมีความหมายว่า “สิ่งที่ไม่สามารถแบ่งแยกได้” และเนื่องจาก “อะตอม” มีขนาดเล็กมากจนไม่สามารถมองเห็นได้ด้วยตาเปล่า แม้จะใช้กล้องจุลทรรศน์ที่มีกำลังขยายสูงก็ยังไม่สามารถเห็นรูปร่างที่แท้จริงของอะตอมได้ นักวิทยาศาสตร์จึงอาศัยข้อมูลจากการทดลองมาสร้าง แบบจำลองอะตอม (atomic model) เพื่ออธิบายลักษณะและการจัดเรียงภายในของอะตอม ซึ่งมักแสดงในรูปของทรงกลมเพื่อให้เข้าใจง่าย แบบจำลองเหล่านี้ช่วยให้เราศึกษาและทำความเข้าใจโครงสร้างของสสารได้ แม้จะยังไม่สามารถมองเห็นอะตอมจริง ๆ ได้ก็ตาม
อะตอมประกอบด้วยอะไรบ้าง
ในเบื้องต้นนักวิทยาศาสตร์ได้มีการคาดการณ์ว่า “อะตอม” ประกอบไปด้วยอนุภาคไฟฟ้าพื้นฐาน 3 อย่าง ได้แก่
โปรตอน (Proton) ที่มีประจุไฟฟ้าเป็นบวก (+1) โดยจะแทนด้วยสัญลักษณ์ p หรือ p+
นิวตรอน (Neutron) ที่มีค่าเป็นกลาง (0) และมีมวลใกล้เคียงกับโปรตอน แทนด้วย n หรือ $ n^0 $
อิเล็กตรอน (Electron) ที่มีประจุไฟฟ้าเป็นลบ (-1) มีขนาดเล็กมากเมื่อเทียบกับโปรตอนและนิวตรอน แทนด้วย e หรือ e–
โดยส่วนของนิวเคลียสที่หนาแน่นมากตรงจุดศูนย์กลางจะประกอบไปด้วยโปรตอนและนิวตรอน ล้อมรอบด้วยอิเล็กตรอนที่ถูกดึงดูดให้อยู่ใกล้กับนิวเคลียสด้วยแรงแม่เหล็กไฟฟ้า ซึ่งอะตอมที่มีคุณสมบัติเป็นกลางทางไฟฟ้าจะมีประจุบวก (โปรตอน) เท่ากับประจุลบ (อิเล็กตรอน)
ทั้งนี้ ในอะตอมที่มีคุณสมบัติเป็นกลางทางไฟฟ้า จะมีจำนวนอิเล็กตรอนและโปรตอนเท่ากัน และมีค่าเท่ากับจำนวน “เลขอะตอม (Atomic Number)” ส่วน “เลขมวล (Mass Number)” คือ จำนวนโปรตอน + จำนวนนิวตรอน ซึ่งเราจะสามารถเขียนสัญลักษณ์เพื่อระบุเลขอะตอมและเลขมวลได้ ดังนี้ ${}^{Z}_{A}\mathrm{X}$
โดยที่ A แทนเลขมวล Z แทนเลขอะตอม และ X แทนสัญลักษณ์ของธาตุ ตัวอย่างเช่น ${}^{11}_{23}\mathrm{Na}$
จะเห็นได้ว่า ธาตุโซเดียม (Na) มีเลขอะตอม = 11 คือ มีจำนวนโปรตอนและอิเล็กตรอน 11 ส่วนเลขด้านบนที่เป็นเลขมวล แสดงถึงจำนวนโปรตอน + จำนวนนิวตรอน ดังนั้นแล้วจำนวนนิวตรอนจะเท่ากัน 23-11 = 12
แปลว่าธาตุโซเดียมมีจำนวนโปรตอน, อิเล็กตรอน และนิวตรอนเท่ากับ 11, 11 และ 12 ตามลำดับ
โดยธาตุแต่ละธาตุก็จะมีจำนวนโปรตอน, นิวตรอน และอิเล็กตรอนที่แตกต่างกันออกไป ทำให้แต่ละธาตุมีสมบัติทางเคมีต่างกันตามไปด้วยนั่นเอง
โมเลกุลคืออะไร ?
Molecule หรือ โมเลกุล คือ กลุ่มของอะตอมตั้งแต่ 2 อะตอมขึ้นไปที่ยึดติดกันด้วย “พันธะทางเคมี” (Chemical Bonds) ที่เป็นตัวก่อให้เกิดการรวมตัวกันของอะตอมจนก่อเกิดเป็นโมเลกุล และเกิดการจับตัวกันกลายเป็นโครงสร้างที่ซับซ้อนมากยิ่งขึ้น
และมีขนาดใหญ่ขึ้น จนกลายเป็นสสาร (matter) ที่ก่อให้เกิดสารประกอบ เนื้อเยื่อ อวัยวะ รวมถึงส่วนประกอบต่าง ๆ ของสิ่งมีชีวิตและสิ่งไม่มีชีวิต ซึ่งสามารถมองเห็นและสัมผัสได้ในโลกจริง โดยพันธะทางเคมีของอะตอมที่ก่อให้เกิดโมเลกุล จะมี 3 รูปแบบ ได้แก่
1. พันธะไอออนิก (Ionic Bond)
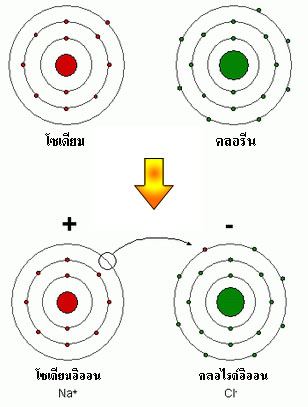
เป็นพันธะที่เกิดขึ้นระหว่างไอออนซึ่งมีประจุตรงข้ามกัน โดยเกิดแรงดึงดูดทางไฟฟ้าระหว่าง ไอออนบวก (cation) และ ไอออนลบ (anion) พันธะชนิดนี้เกิดขึ้นจากการ ถ่ายโอนอิเล็กตรอนหนึ่งตัวหรือมากกว่า จากอะตอมหนึ่งไปสู่อีกอะตอมหนึ่ง ทำให้ทั้งสองอะตอมมีโครงสร้างอิเล็กตรอนชั้นนอกสุดที่ ครบออกเตต (Octet rule) และเสถียรมากขึ้น
พันธะไอออนิกเกิดขึ้นระหว่างอะตอมของโลหะและอโลหะ โดยอะตอมโลหะจะถ่ายโอนอิเล็กตรอนให้แก่อะตอมอโลหะ ตัวอย่างเช่น อะตอมโซเดียม (Na) ถ่ายโอนอิเล็กตรอนวงนอกสุด 1 ตัวให้แก่อะตอมคลอรีน (Cl) ทำให้เกิดไอออนโซเดียมประจุบวก (Na⁺) และไอออนคลอรีนประจุลบ (Cl⁻) ทั้งสองไอออนดึงดูดกันด้วยแรงไฟฟ้า เกิดเป็นสารประกอบโซเดียมคลอไรด์ (NaCl) หรือเกลือ
2. พันธะโคเวเลนท์ (Covalent Bond)
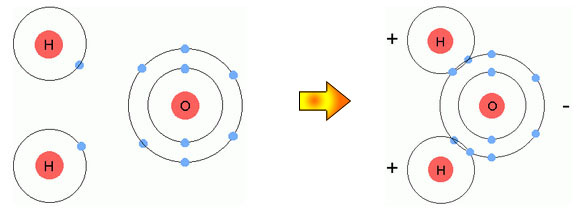
พันธะโควาเลนต์ (Covalent bond) เกิดจากการที่อะตอมใช้อิเล็กตรอนวงนอกคู่หนึ่งหรือหลายคู่ร่วมกัน โดยทั่วไปเกิดระหว่างอะตอมของอโลหะ ซึ่งมีค่า Electronegativity และ Ionization energy สูง การใช้อิเล็กตรอนร่วมกันช่วยให้อะตอมแต่ละตัวมีอิเล็กตรอนวงนอกครบตามกฎออกเตต (Octet rule) พันธะอาจเป็นพันธะเดี่ยว (ใช้อิเล็กตรอนร่วมกัน 1 คู่) พันธะคู่ (ใช้อิเล็กตรอนร่วมกัน 2 คู่) หรือพันธะสาม (ใช้อิเล็กตรอนร่วมกัน 3 คู่) ก็ได้
ตัวอย่าง: โมเลกุลน้ำ (H2O) เกิดจากอะตอมออกซิเจนจับกับอะตอมไฮโดรเจนสองอะตอมด้วยพันธะโควาเลนต์เดี่ยวแบบมีขั้ว (polar covalent bond)
3. พันธะโลหะ (Metallic Bond)
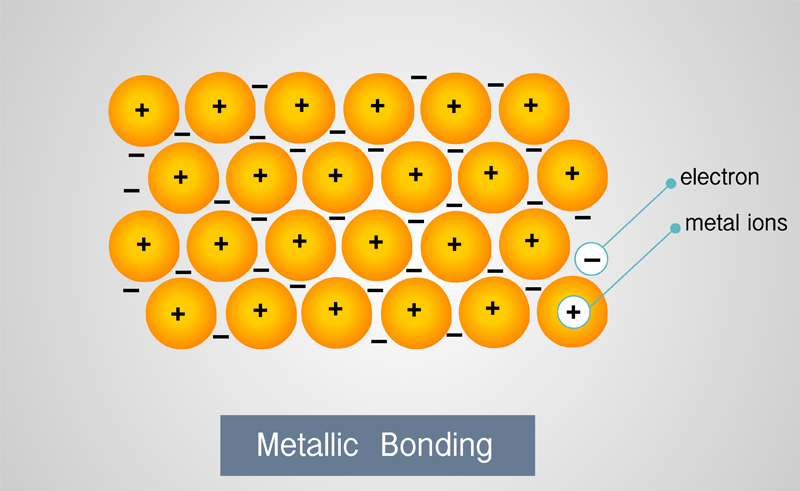
พันธะโลหะ (Metallic bond) เป็นพันธะที่เกิดขึ้นระหว่างอะตอมของธาตุโลหะ โดยอะตอมโลหะแบ่งปันอิเล็กตรอนวงนอกสุดร่วมกันในลักษณะ “ทะเลอิเล็กตรอน” (sea of electrons) อิเล็กตรอนเหล่านี้สามารถเคลื่อนที่ได้อย่างอิสระทั่วทั้งโครงสร้างของโลหะ ทำให้โลหะสามารถนำไฟฟ้า นำความร้อน และตีเป็นแผ่นหรือดึงเป็นเส้นได้ง่าย
ตัวอย่าง: อะตอมของเหล็ก (Fe) รวมตัวกันด้วยพันธะโลหะเกิดเป็นแท่งเหล็ก ซึ่งไม่มีจำนวนอะตอมแน่นอน และสามารถนำกระแสไฟฟ้าได้ทั่วทั้งแท่ง
จากตัวอย่างที่ยกมา จะเห็นได้ว่า อะตอมที่ยึดเหนี่ยวกันจนเกิดเป็นโมเลกุล อาจเป็นอะตอมของธาตุเดียวกันหรือคนละธาตุกันก็ได้ ทั้งนี้สามารถสังเกตได้จาก สูตรโมเลกุล (Molecular formula) ซึ่งแสดงชนิดและจำนวนของอะตอมที่เป็นองค์ประกอบของโมเลกุลนั้น ๆ
- โมเลกุลของธาตุเดียวกัน เช่น C₂ ประกอบด้วยอะตอมของคาร์บอน (C) จำนวน 2 อะตอม
- โมเลกุลของสารประกอบ เช่น H₂O ประกอบด้วยอะตอมของไฮโดรเจน (H) 2 อะตอม และอะตอมของออกซิเจน (O) 1 อะตอม
ดังนั้นโมเลกุลที่เกิดจากการรวมตัวของอะตอมต่างชนิดกันจะเรียกว่า สารประกอบ (Compound)
โมเลกุลกับอะตอมต่างกันอย่างไร
อะตอม คือ อนุภาคที่เล็กที่สุดของธาตุ ส่วนโมเลกุล คือ กลุ่มของอะตอมตั้งแต่สองอะตอมขึ้นไปที่ยึดเหนี่ยวกันด้วยพันธะเคมี เมื่อโมเลกุลจำนวนมากรวมตัวกัน จะเกิดเป็น สสาร ที่สามารถมองเห็นได้ด้วยตาเปล่า เช่น น้ำ (H2O) ที่เกิดจากการรวมตัวของโมเลกุลน้ำจำนวนมากจนกลายเป็นหยดน้ำ
ตัวอย่างข้อสอบ GED Science ในหัวข้อโมเลกุลและอะตอม
Which of the following is NOT a subatomic particle found inside the atom?
- Protons
- Neutrons
- Ions
- Electrons
ข้อนี้ตอบ C เพราะ “อะตอม” ประกอบไปด้วยอนุภาคพื้นฐานทางไฟฟ้า 3 อย่าง ได้แก่ โปรตอน, นิวตรอน และอิเล็กตรอน นั่นเอง
เทคนิคสำคัญพิชิตข้อสอบ GED Science อะตอมและโมเลกุล ในหัวข้อ Physical Science
เป็นยังไงบ้างกับการทำความเข้าใจความต่างและความหมายว่าทั้งอะตอมและโมเลกุลคืออะไร พี่กริฟฟินหวังเป็นอย่างยิ่งว่าน้อง ๆ จะทำข้อสอบ GED Science ที่ไม่ใช่ข้อสอบแบบ “ท่องจำ” แต่จะเน้นการวัดทักษะด้านการตีความ การจับใจความสำคัญ และการอนุมานสมมติฐานทางวิทยาศาสตร์ได้คล่องขึ้น สิ่งสำคัญคือไม่จำเป็นต้องท่องตารางธาตุหรือส่วนประกอบของธาตุต่าง ๆ เพื่อเตรียมสอบ แต่ให้ใช้ความเข้าใจเกี่ยวกับเครื่องหมายและสัญลักษณ์ต่าง ๆ ในเชิงวิทยาศาสตร์ที่เป็นส่วนประกอบเป็นหลัก นอกจากนี้ข้อสอบบางข้อยังเป็น Passage หรือบทความที่มีคำตอบซ่อนอยู่ภายในเนื้อหาอยู่แล้ว หากเข้าใจว่า “โจทย์ต้องการถามอะไร” ก็สามารถหาคำตอบได้ไม่ยาก นอกจากทำความเข้าใจโจทย์ให้ดีแล้ว น้อง ๆ อย่าลืมแบ่งเวลาการอ่านสอบให้ครอบคลุมเนื้อหาการสอบทั้ง 3 หัวข้อของข้อสอบ GED Science ให้ครบถ้วน เพื่อที่จะได้ลงสอบผ่านได้ในครั้งเดียวแบบไม่ต้องลงสอบซ้ำ
สามารถดู Study Guide ของข้อสอบ GED Science พร้อมตัวอย่างข้อสอบและเฉลยเบื้องต้นได้ ที่นี่
ติวเสริมเพิ่มความมั่นใจก่อนลงสอบจริงไปกับ House of Griffin
หากใครไม่มั่นใจและต้องการผู้ช่วยติวสอบ GED ก็สามารถลงติวเสริมกับ House of Griffin สถาบันติวสอบ GED ที่มีประสบการณ์กว่า 14 ปีและผ่านการรับรองมาตรฐานหลักสูตรจาก GED Official ของสหรัฐอเมริกาให้เป็น Authorized GED Test Prep Provider แห่งแรกในประเทศไทยและในเอเชีย มีคอร์สติว GED แบบครอบคลุมทั้ง 4 รายวิชา ทั้ง GED Science, GED RLA, GED Math และ GED Social Studies เก็บครบทุกเทคนิคพิชิตข้อสอบ พร้อมตะลุยคลังโจทย์ข้อสอบฝึกการบริหารเวลาและการทำความเข้าใจโจทย์แบบลึกซึ้ง สอบผ่านครบจบในครั้งเดียว การันตีคว้าวุฒิ GED มาครองได้ในระยะเวลาเพียง 2 เดือน (เงื่อนไขเป็นไปตามที่สถาบันกำหนด)



